Achtergrond
Het folliculair lymfoom wordt ingedeeld naar het aantal centroblasten per high power field (hpf; tabel 1). Het merendeel (> 80%) van de folliculaire lymfomen is graad 1-2 (< 15% centroblasten). In het geval van graad 3a (meer dan 15% centroblasten per hpf) is het beleid qua behandeling en prognose niet eenduidig. Bij een sterke toename aan blasten met solide velden van blasten zal in de grote meerderheid sprake zijn van een folliculair graad 3B, of zelfs een diffuus grootcellig B-cellymfoom met folliculair lymfoom.
| Graad | % centroblasten | Gedrag |
|---|---|---|
| Graad 1 | < 5/hpf | Indolent |
| Graad 2 | 6-15/hpf | Indolent |
| Graad 3a | > 15/hpf | Intermediate |
| Graad 3b | Follikels met blastaire cellen | Agressief |
Prognose
Prognose kan worden bepaald aan de hand van de FLIPI (Buske et al.). Laag risico (0-1), intermediair (2) en hoog (3-5) hebben een 10-jaarsoverleving van respectievelijk 70%, 50% en 35%. Hoewel er moleculair subgroepen gedefinieerd kunnen worden met een hoog risico (m7 FLIPI) wordt dit niet routinematig gebruikt (Pastore et al.). De belangrijkste voorspeller voor langetermijnuitkomsten voor patiënten die een behandeling dienen te ondergaan is de 2-jaars PFS (Casulo et al.).
| Prognostische factor | Aantal punten |
|---|---|
| Leeftijd > 60 jaar | 1 |
| Stadium III/IV | 1 |
| Aantal klierstations > 4* | 1 |
| LDH > ULN | 1 |
| Hb < 7,5 mmol/l | 1 |
Behandeling
Filter trials en protocollen voor dit ziektebeeldStadium I
In opzet curatieve radiotherapie.
Stadium II-IV
Behandelindicatie bij beenmergverdringing met cytopenie en/of aanwezigheid van een van de volgende criteria (GELF criteria):
- Nodale of extranodale tumor met diameter > 7 cm
- B-symptomen
- Verhoogd serum LDH
- Aantasting ≥ 3 nodale lokalisaties (elk met een diameter > 3 cm)
- Symptomatische splenomegalie
- Compressiesyndroom (ureter, galweg, trachea, etc.)
- Pleurale, peritoneale effusie
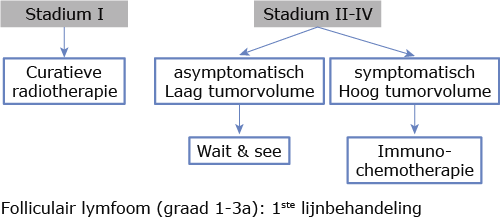
Chemo-immunotherapie
Bij de keuze voor chemo-immunotherapie zijn er meerdere behandelopties. Bij lage FLIPI-score of patiënten met comorbiditeit gaat de voorkeur uit naar R-COP kuren. Bij hoog FLIPI gaat de voorkeur uit naar R-CHOP, dan wel R-bendamustine.
| Stadium | leeftijd | Behandeling |
|---|---|---|
| I | Alle leeftijden | IF-RT 36 Gy |
| II (beperkt) | Alle leeftijden | IF-RT 36 Gy |
| (II) III, IV | Alle leeftijden (geen sympt) | Wait en see [1] |
| Alle leeftijden: Behandelindicatie (FLIPI 1-3) Behandelindicatie (FLIPI 3-5) Oudere patiënt |
8 × R-CVP [2] 6 × R-CHOP [3] 6 × R-benadmustine [3] R-chloorambucil [4] Evt. rituximab monotherapie [5] |
Onderhoudsbehandeling
Onderhoudsbehandeling met rituximab na eerstelijns inductiebehandeling laat een verbetering zien in de progressievrije overleving, echter geen overtuigend voordeel in overall survival (na 6 jaar: 42,7% versus 59,2% (p < 0,0001; HR 0,58) OS est 6 jaar: 88,7% versus 87,4% [6]. Een systemische meta-analyse toonde aan dat onderhoudsbehandeling met rituximab bij patiënten met recidief ziekte een substantieel verlenging hadden met betrekking tot PFS en OS [1, 7]. Derhalve starten we met onderhoud na tweedelijnsbehandeling. Onderhoudsbehandeling gaat overigens wel gepaard met meer graad 3 en 4 toxiciteit (HR 1,31, 95% CI 1160 1,08-1,58) en een verhoogd risico op infecties (HR 1,41, 95% CI 1,20-1,66), met ook een duidelijke toename in graad 3 en 4 infectieuze complicaties (HR 1,548, 95% CI 1,04-2,11).
Behandeling recidief folliculair lymfoom
Buiten studieverband (zie figuur 1)
De behandeling is afhankelijk van de tot dan toe gegeven behandelingen. Bij lange responsduur kan het tot dan toe meest succesvolle regime opnieuw gegeven worden (met uitzondering van anthracyclines). Mogelijkheden zijn:
- 6× R-CHOP in geval van CR/PR evt. met onderhoudsbehandeling (elke 3 maanden gedurende maximaal 2 jaar) [8]
- Bendamustine + anti-CD20 therapie [3, 9]
- Bij patiënten ≤ 65 jaar kan salvage chemotherapie ((R) DHAP-VIM-DHAP) gevolgd door een autologe SCT worden overwogen
- Idelalisib [10]
- Radiotherapie (2×2 Gy) [11]
- Radioimmunotherapie: Zevalin [12]
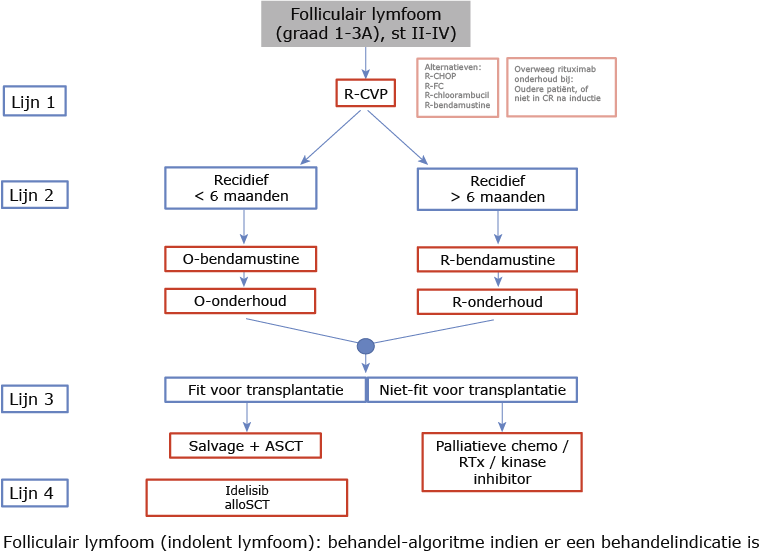
Indien patiënten een recidief/progressie krijgen tijdens of binnen 6 maanden na rituximab-bevattende immunochemotherapie of onderhoudsbehandeling worden zij beschouwd als rituximab-refractair. In het algemeen wordt geadviseerd geen rituximab te geven indien rituximab-refractair. Derhalve adviseren we dan obinutuzimab (met eventueel obinutuzumab-onderhoud). Indien responsduur op voorgaande therapie > 6 maanden is, dan kan in tweedelijnstherapie wederom R-chemo gebruikt worden.
Allogene stamceltransplantatie
- Na 2e of volgende recidief bij een jonge patiënt kan bij korte responsduur op eerdere immunochemotherapie een allogene SCT worden overwogen.
Studies
HOVON 110: ReBeL studie
Fase 2 studie
A randomized phase I/II trial of lenalidomide and rituximab with or without bendamustine in patients ≥ 18 years with relapsed follicular lymphoma. A HOVON/GLSG study.
Samenvatting inclusiecriteria:
- Recidief FL grade 1, 2, 3a
- Ann Arbor stadium II-IV bij recidief
- Bewezen CD20 positief na laatste therapie
- Maximaal 3 eerdere behandellijnen
Paradigm study
Fase 2 studie
A phase I/II study of lutetium (177Lu)-lilotomab satetraxetan (Betalutin®) antibodyradionuclide-conjugate for treatment of relapsed non-Hodgkin lymphoma
Samenvatting inclusiecriteria:
- Recidief FL graad 1, 2, 3a
- Minimaal 2 lijnen chemo-immunotherapie gehad
- Refractair op de laatste anti-CD20 gebaseerde behandeling
- Minder dan 25% tumorinfiltratie in het beenmerg
Folliculair lymfoom graad 3B en getransformeerd lymfoom
Het advies is om deze type lymfomen te behandelen als diffuus grootcellig B-cellymfoom met R-CHOP (zie aldaar). In het geval van twijfel (graad 3A, indolent klinisch gedrag, geen additionele cytogenetische afwijkingen) is het gerechtvaardigd een beleid te hanteren zoals voor een indolent lymfoom. Wanneer de kliniek echter een agressiever lymfoom doet vermoeden, overweeg dan een nieuw biopt te laten nemen zo nodig op geleide van de PET-scan.
Kuurschema’s
| R-CVP à 3 weken | dosis | dag |
|---|---|---|
| Rituximab | 375 mg/m2 i.v. | 1 |
| Cyclofosfamide | 750 mg/m2 i.v. | 1 |
| Vincristine | 2 mg i.v. | 1 |
| Prednison | 100 mg p.o. | 1-5 |
| R-bendamustine à 4 weken | dosis | dag |
|---|---|---|
| Rituximab | 375 mg/m2 i.v. | 1 |
| Bendamustine | 70-90 mg/m2 i.v. | 1, 2 |
| R-CHOP à 3 weken | dosis | dag |
|---|---|---|
| Rituximab | 375 mg/m2 i.v. | 1 |
| Cyclofosfamide | 750 mg/m2 i.v. | 1 |
| Doxorubine | 50 mg/m2 i.v. | |
| Vincristine | 2 mg i.v. | 1 |
| Prednison | 100 mg p.o. | 1-5 |
| R-FC à 4 weken | dosis | dag |
|---|---|---|
| Rituximab | 375 mg/m2 i.v. | 1 |
| Cyclofosfamide | 250 mg/m2 i.v. | 1-3 |
| Fludarabine | 40 mg/m2 i.v. | 1-3 |
Literatuurlijst
- Dreyling M, Ghielmini M, Rule S, Salles G, Vitolo U, Ladetto M, ESMO Guidelines Committee. Newly diagnosed and relapsed follicular lymphoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2016; 27: v83–v90. doi: 10.1093/annonc/mdw400.
- Marcus R, Imrie K, Solal-Celigny P, Catalano JV, Dmoszynska A, Raposo JC, Offner FC, Gomez-Codina J, Belch A, Cunningham D, Wassner-Fritsch E, Stein G. Phase III study of R-CVP compared with cyclophosphamide, vincristine, and prednisone alone in patients with previously untreated advanced follicular lymphoma. J Clin Oncol. 2008; 26: 4579–86. doi: 10.1200/JCO.2007.13.5376.
- Rummel MJ, Niederle N, Maschmeyer G, Banat GA, Grünhagen von U, Losem C, Kofahl-Krause D, Heil G, Welslau M, Balser C, Kaiser U, Weidmann E, Dürk H, et al. Bendamustine plus rituximab versus CHOP plus rituximab as first-line treatment for patients with indolent and mantle-cell lymphomas: an open-label, multicentre, randomised, phase 3 non-inferiority trial. Lancet. 2013; 381: 1203–10. doi: 10.1016/S0140-6736(12)61763-2.
- Martinelli G, Montoro J, Vanazzi A, Andreola G, Liptrott S, Radice D, Negri M, Preda L, Pruneri G, Laszlo D. Chlorambucil-rituximab as first-line therapy in patients affected by follicular non-Hodgkin’s lymphoma: a retrospective single-centre study. Hematological Oncology. 4 ed. 2015; 33: 129–35. doi: 10.1002/hon.2154.
- Martinelli G, Schmitz S-FH, Utiger U, Cerny T, Hess U, Bassi S, Okkinga E, Stupp R, Stahel R, Heizmann M, Vorobiof D, Lohri A, Dietrich P-Y, et al. Long-term follow-up of patients with follicular lymphoma receiving single-agent rituximab at two different schedules in trial SAKK 35/98. J Clin Oncol. 2010; 28: 4480–4. doi: 10.1200/JCO.2010.28.4786.
- Salles G, Seymour JF, Offner F, López-Guillermo A, Belada D, Xerri L, Feugier P, Bouabdallah R, Catalano JV, Brice P, Caballero D, Haioun C, Pedersen LM, et al. Rituximab maintenance for 2 years in patients with high tumour burden follicular lymphoma responding to rituximab plus chemotherapy (PRIMA): a phase 3, randomised controlled trial. Lancet. 2011; 377: 42–51. doi: 10.1016/S0140-6736(10)62175-7.
- Vidal L, Gafter-Gvili A, Salles G, Bousseta S, Oberman B, Rubin C, van Oers MHJ, Fortpied C, Ghielmini M, Pettengell R, Witzens-Harig M, Dreger P, Vitolo U, et al. Rituximab maintenance improves overall survival of patients with follicular lymphoma-Individual patient data meta-analysis. Eur J Cancer. 2017; 76: 216–25. doi: 10.1016/j.ejca.2017.01.021.
- van Oers MHJ, Klasa R, Marcus RE, Wolf M, Kimby E, Gascoyne RD, Jack A, Van’t Veer M, Vranovsky A, Holte H, van Glabbeke M, Teodorovic I, Rozewicz C, et al. Rituximab maintenance improves clinical outcome of relapsed/resistant follicular non-Hodgkin lymphoma in patients both with and without rituximab during induction: results of a prospective randomized phase 3 intergroup trial. Blood. American Society of Hematology; 2006; 108: 3295–301. doi: 10.1182/blood-2006-05-021113.
- Sehn LH, Chua N, Mayer J, Dueck G, Trneny M, Bouabdallah K, Fowler N, Delwail V, Press O, Salles G, Gribben J, Lennard A, Lugtenburg PJ, et al. Obinutuzumab plus bendamustine versus bendamustine monotherapy in patients with rituximab-refractory indolent non-Hodgkin lymphoma (GADOLIN): a randomised, controlled, open-label, multicentre, phase 3 trial. Lancet Oncol. 2016; 17: 1081–93. doi: 10.1016/S1470-2045(16)30097-3.
- Gopal AK, Kahl BS, de Vos S, Wagner-Johnston ND, Schuster SJ, Jurczak WJ, Flinn IW, Flowers CR, Martin P, Viardot A, Blum KA, Goy AH, Davies AJ, et al. PI3Kδ inhibition by idelalisib in patients with relapsed indolent lymphoma. N Engl J Med. Massachusetts Medical Society; 2014; 370: 1008–18. doi: 10.1056/NEJMoa1314583.
- Ganem G, Cartron G, Girinsky T, Haas RLM, Cosset JM, Solal-Celigny P. Localized low-dose radiotherapy for follicular lymphoma: history, clinical results, mechanisms of action, and future outlooks. Int J Radiat Oncol Biol Phys. 2010; 78: 975–82. doi: 10.1016/j.ijrobp.2010.06.056.
- Witzig TE, Molina A, Gordon LI, Emmanouilides C, Schilder RJ, Flinn IW, Darif M, Macklis R, Vo K, Wiseman GA. Long-term responses in patients with recurring or refractory B-cell non-Hodgkin lymphoma treated with yttrium 90 ibritumomab tiuxetan. Cancer. Wiley Subscription Services, Inc., A Wiley Company; 2007; 109: 1804–10. doi: 10.1002/cncr.22617.




