Acute myeloïde leukemie (AML)
Acute myeloïde leukemie (AML) is een onderdeel van de acute leukemieën. Onder acute leukemie (ook wel bloedkanker genoemd) wordt een levensbedreigend ziektebeeld verstaan waarbij in korte tijd (dagen tot weken) een snelle woekering van kwaadaardige leukemiecellen (blasten) de plaats inneemt van de normale bloedaanmaak. De normale bloedaanmaak speelt zich af in het beenmerg (zie ook Beenmergonderzoek) (zie dia 2 en 3). Daarbij worden de verschillende celsoorten aangemaakt, zoals de rode cellen (nodig voor zuurstoftransport; een tekort leidt tot bloedarmoede), de witte cellen (leukocyten genaamd; er zijn veel verschillende soorten en ze zijn nodig voor de afweer tegen bacteriën, virussen en andere infectiebronnen) en bloedplaatjes (trombocyten genaamd, nodig voor de bloedstolling).

Dia 1
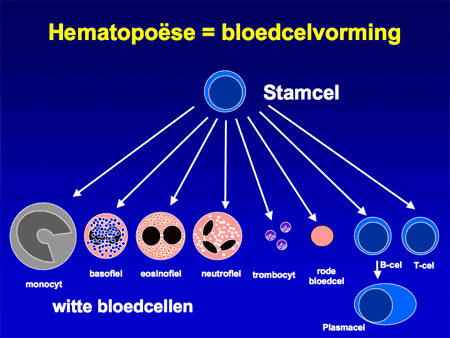
Dia 2
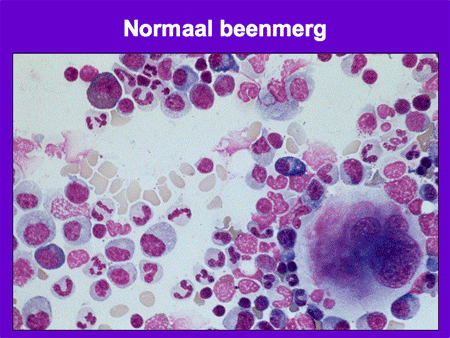
Dia 3
Wanneer normaal beenmerg, na een beenmergpunctie verkregen, onder de microscoop bekeken wordt, is er een heel divers beeld te zien van alle verschillende celsoorten (zie dia 3). In het geval van acute leukemie zijn vrijwel alle normale beenmergelementen vervangen door de blasten (zie dia 4). Het ziektebeeld leukemie kenmerkt zich dan ook vooral door het feit dat er enerzijds een teveel is aan leukemiecellen en anderzijds een tekort aan de normale bloedelementen (zie dia 5).
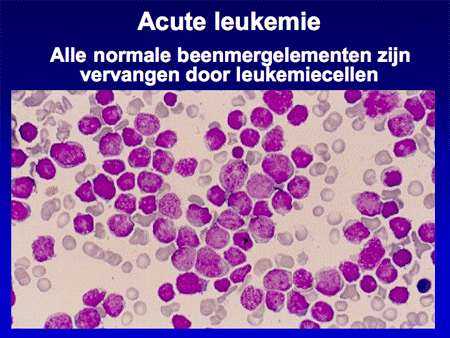
Dia 4. Bij acute leukemie zijn vrijwel alle normale beenmergelementen vervangen door leukemiecellen

Dia 5
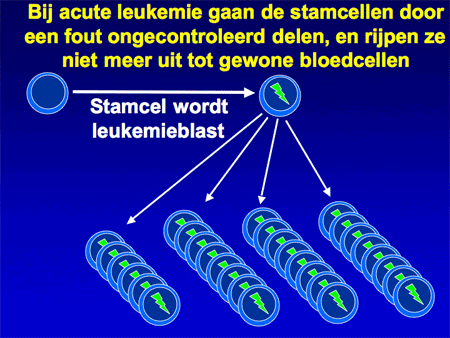
Dia 6
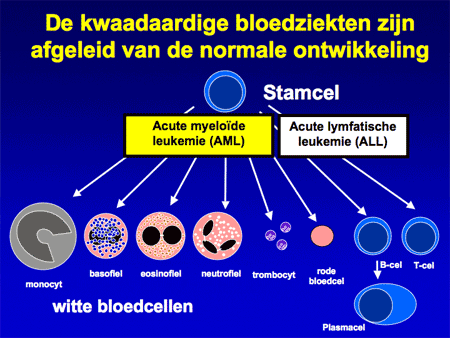
Dia 7
Hoe ontstaat acute leukemie en hoe vaak komt het voor?
Aangenomen wordt dat de kwaadaardige cellen bij acute leukemie ontstaan op het niveau van de vroegste ontwikkeling van de normale bloedcellen, de stamcellen (zie dia 6). Ergens tijdens de deling van die bloedstamcellen gaat iets mis, waardoor de cellen harder gaan delen en bovendien ook niet meer uitrijpen tot normale bloedcellen (zie dia 7).
We weten niet hoe acute myeloïde leukemie kan ontstaan. De grote meerderheid ontstaat ‘zomaar’, zonder dat de reden bekend is. In het zeldzame geval dat er wel een verklaring lijkt te zijn, gaat het om oorzaken als straling of bepaald medicamentengebruik. AML kan ontstaan na straling, zoals gezien is na de atoombommen in Japan. Ook zijn er bepaalde stoffen (zoals benzeen) en celdodende medicijnen (gebruikt als antikankerbehandeling, chemotherapie) die op hun beurt weer acute leukemie kunnen veroorzaken.
Acute leukemie is erg zeldzaam en wordt per jaar bij ongeveer 4 patiënten per 100.000 inwoners in Nederland geconstateerd. Van de twee verschillende soorten – acute myeloïde (AML) en acute lymfatische leukemie (ALL) – komt ALL vooral bij kinderen voor, hoewel ALL net zo goed ook bij volwassenen voorkomt. AML is veel meer een ziekte van volwassenen.
Hoe wordt de diagnose gesteld?
Patiënten met acute leukemie hebben vrijwel altijd klachten en symptomen die veroorzaakt zijn door het teveel aan leukemiecellen en het tekort aan normale cellen. Door de bloedarmoede kan algemene zwakte en bleekheid met onverklaarbare, toenemende vermoeidheid gezien worden. Door het tekort aan witte cellen kunnen veelvuldig terugkerende kleine infecties en koorts ontstaan. Door het tekort aan bloedplaatjes ontstaan gemakkelijk blauwe plekken of bloedingen, bijvoorbeeld neusbloedingen, kleine huidbloedingen (kleine rode stipjes op het lichaam) of tandvleesbloedingen (bijvoorbeeld bij het tandenpoetsen).
Bloed- en beenmergonderzoek is voldoende om de diagnose te stellen. Aan dit onderzoek zijn wel voorwaarden verbonden. Het materiaal moet op een speciale manier verwerkt worden om alle specifieke kleuringen, waaronder ook flowcytometrie (zie flowcytometrie), op de cellen te kunnen verrichten. Daarnaast is bij AML ook chromosomenonderzoek zeer belangrijk. Deze extra technieken zijn nodig om de leukemie beter te kunnen classificeren (zie dia 9). Bovendien is het hiermee mogelijk om een betere schatting te maken van de prognose. Sommige leukemieën hebben een agressiever beloop of zijn moeilijker te behandelen dan andere vormen. Vaak betekent dit daarom dat het beenmergonderzoek overgedaan moet worden als een patiënt verwezen wordt naar een centrum voor behandeling.

Dia 8

Dia 9
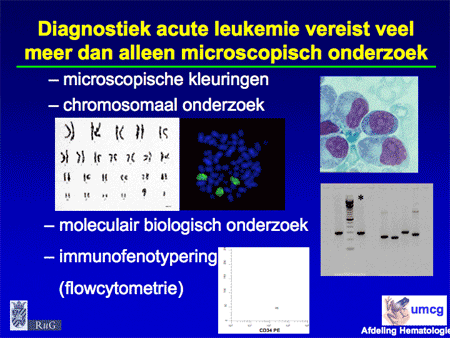
Dia 10. Bij AML is naast microscooponderzoek ook flowcytometrie en chromosomenonderzoek nodig
Bij AML wordt er onderscheid gemaakt tussen vijf grote groepen:
- AML met specifieke chromosoomafwijkingen;
- AML met bijkomende dysplasie;
- AML (of MDS) in relatie tot vroegere chemo- of radiotherapie;
- AML overige;
- acute leukemie met kenmerken van zowel ALL als AML.
Wat de soorten AML uit groep 1 (een kleine groep) betreft, zijn er subgroepen die een veel beter beloop hebben dan de grote groep andere AML-soorten. Eén specifieke soort is de zogenaamde promyelocytenleukemie. Deze wordt apart beschreven in Acute promyelocytenleukemie, omdat voor deze subgroep aparte therapie wordt toegediend. Voor het overige is het tot nu toe nog niet zinvol gebleken specifieke therapie te geven, maar de hoop is dat dit in de toekomst wel het geval zal zijn. Het voordeel van deze AML-indeling is dat alle hematologen dezelfde taal spreken wanneer gegevens van verschillende patiënten met elkaar vergeleken worden.
Therapie AML
Aangezien AML een ziekte is van vooral oudere patiënten, wordt allereerst onderscheid gemaakt tussen patiënten ouder of jonger dan circa 65 tot 70 jaar. De oudere leeftijdsgroep wordt bij voorkeur buiten het ziekenhuis behandeld met lichtere therapie. AML bij ouderen heeft soms een wat milder beloop en is aan de andere kant moeilijker te behandelen, laat staan te genezen. Oudere patiënten blijken de therapie zoals die aan jongeren gegeven wordt, vaak ook slecht te verdragen. Het is niet alleen de leeftijd die hierbij doorslaggevend is, ook de fitheid (de algemene conditie, de zelfredzaamheid, de aan- of afwezigheid van andere aandoeningen zoals suikerziekte, longafwijkingen en hartzieken) bepaalt wat een patiënt voor behandeling aankan.
Allereerst volgt hier een algemene uitleg. Daarna wordt de specifieke therapie bij acute myeloïde leukemie besproken.
Behandeling van acute leukemie bij patiënten jonger dan 60-65 jaar
Om de kwaadaardige cellen kwijt te raken moeten patiënten behandeld worden met hoge doses celdodende medicijnen (chemotherapie). Deze medicijnen zullen de leukemiecellen doden, maar tijdelijk ook de gewone bloedcellen in het beenmerg. Dit komt omdat leukemiecellen erg lijken op normale bloedcellen en de celdodende medicijnen het onderscheid niet goed kunnen zien. Gelukkig zijn normale bloedcellen meestal sterker dan leukemiecellen. Het gevolg is dat de normale bloedcellen vanuit de enkele achtergebleven gezonde stamcellen weer zullen uitrijpen, terwijl de leukemiecellen hopelijk zijn uitgeschakeld.
Er moet echter – per behandelingsperiode, en er zijn er meerdere! – wel steeds een gevaarlijke periode van enkele weken overbrugd worden waarin de bloedcelaanmaak stilligt en de patiënt geen eigen rode cellen, witte cellen en bloedplaatjes aanmaakt. Acute leukemiepatiënten hebben bij de start al een slechte weerstand door de aantasting van hun normale bloedcelaanmaak. Door de chemotherapie zal deze weerstand dus nog verder verslechteren. Voor een dergelijke behandeling met chemotherapie moeten patiënten dan ook opgenomen worden in het ziekenhuis, bij voorkeur in een centrum met een beschermde afdeling dat in staat is dit soort zware therapie te geven. In het UMCG is de gehele verpleegafdeling E2VA beschermd, inclusief de gangen en vierpersoonskamers. Dit betekent dat het niet altijd nodig is een patiënt met acute leukemie op een eenpersoonskamer te verplegen. Omdat chemotherapie schadelijk kan zijn voor gezonde personen, zoals het verpleegkundig personeel, worden op de afdeling regels voor het omgaan met besmet materiaal gehanteerd om hen zo veel mogelijk te beschermen.
Voordat gestart kan worden met de behandeling, zal eerst onderzocht worden of een patiënt nog infecties bij zich draagt die tijdens de behandeling een probleem zouden kunnen geven. Het gaat dan om infecties vanuit de neus, keel en longen en vooral om infecties vanuit het gebit. In het UMCG zullen de patiënten daarom uitgebreid onderzocht worden door de keel-neus-oren (KNO)-arts en door de kaakchirurg/tandarts, en ook tijdens de behandeling begeleid worden door de mondhygiënist(e). Heel vaak blijkt het helaas noodzakelijk om enkele gebitselementen te verwijderen, omdat deze anders tijdens de behandeling met chemotherapie problemen zouden kunnen geven.
Behalve de chemotherapie worden beschermende antibiotica gegeven om de weerstand in het lichaam, vooral in de mond en in de darmen, te verhogen. Deze antibioticacombinatie wordt selectieve darmdecontaminatie genoemd. Het tekort aan rode cellen en bloedplaatjes (trombocyten) wordt opgevangen door regelmatig bloedtransfusies te geven.
Door de chemotherapie kan misselijkheid ontstaan en kunnen de slijmvliezen erg geïrriteerd raken. Eten is dan moeilijk, terwijl het extra belangrijk is dat de voedingstoestand van een patiënt op peil blijft. Er zijn rond de voeding een aantal adviezen, zowel over de kwaliteit ervan als de voedingswaarde. Samen met de diëtist(e) wordt zo nodig dagelijks bekeken hoe de voedingstoestand van een patiënt zo goed mogelijk op peil blijft. Er worden daarbij richtlijnen gehanteerd waarbij bepaalde voedingsmiddelen minder gewenst zijn, omdat ze bijvoorbeeld voedselinfecties kunnen veroorzaken bij patiënten met verminderde weerstand. Als het niet goed lukt om voldoende voeding naar binnen te krijgen, zal overgegaan worden op voeding via de bloedbaan (zogenaamde TPN, totale parenterale nutritie). Om deze voeding veilig toe te kunnen dienen is het nodig over een goede toegang tot de bloedbaan te beschikken. Bij voorkeur wordt hiervoor een speciaal aangelegd infuus (centraal veneuze katheter) gebruikt dat ingebracht wordt onder het sleutelbeen. Dit infuus wordt – voordat met de chemotherapie gestart wordt – op de afdeling ingebracht door een van de hematologen onder zo steriel mogelijke omstandigheden. Daarna wordt de insteekopening van het infuus regelmatig door de verpleegkundigen schoongemaakt en goed gecontroleerd op het ontstaan van infecties. Helaas raakt ook een dergelijk infuus nog wel eens besmet en dan zal het weer verwijderd moeten worden.
Patiënten kunnen zich moe en aangeslagen voelen door de behandeling. Desalniettemin is het van het grootste belang dat de conditie zo goed mogelijk blijft. Hoe meer een patiënt uit bed is, hoe beter. Door middel van een hometrainer (fiets of loopband) is het mogelijk de conditie zo goed en kwaad als het kan op peil te houden. De afdeling heeft een speciaal fitness programma ontwikkeld om in goede conditie te blijven en de spieren op kracht te houden – E2 on the move. Daarnaast is het ook belangrijk dat de geestelijke conditie goed blijft. De krant lezen, het journaal volgen en contact onderhouden met de omgeving (er zijn computerlaptops op de afdeling, met internetaansluiting) worden van harte gestimuleerd.
Een overzicht van zo’n kuur met alle voorzorgsmaatregelen is te zien op dia 11.
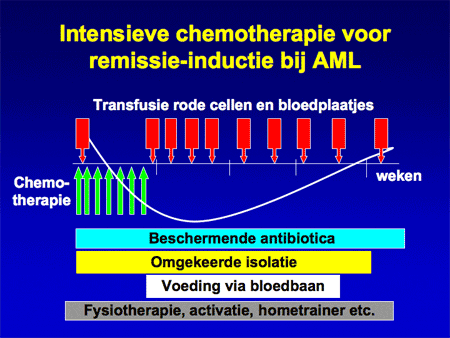
Dia 11

Dia 12
Specifieke behandeling van acute myeloïde leukemie
De behandeling van AML is anders dan die van ALL. De behandeling duurt een aantal maanden, waarbij achter elkaar drie tot vier kuren worden toegediend.
De eerste kuur, waarbij gedurende een week tot tien dagen dagelijks chemotherapie wordt gegeven, heet inductiekuur: de kuur ‘induceert’ een verdwijnen van de leukemie. Na de chemotherapieperiode is het wachten geblazen, waarbij het normale beenmerg weer moet uitgroeien, terwijl de leukemie hopelijk wegblijft. Deze wachtperiode duurt (na het einde van de laatste chemotherapiedag) zo’n drie weken. In die periode is het risico op complicaties het grootst (zie hierboven). Halverwege deze periode wordt een ‘dag 21’ beenmerg onderzocht om te zien of de leukemie al een beetje reageert. Als het beenmerg op dat moment nog vol leukemie zou blijken te zitten, heeft het immers niet veel zin te wachten op herstel en is het beter om meteen door te gaan met een tweede kuur. Gelukkig is dit maar zelden noodzakelijk.
Aan het eind van de inductiekuur zal – op het moment dat het beenmerg hersteld is en de bloedgetallen weer goed stijgen – een beenmergonderzoek gedaan worden om dan definitief vast te stellen of er na deze eerste kuur een complete remissie (verdwijnen van de leukemie) is opgetreden. Een complete remissie klinkt overigens mooier dan het is: het wil alleen maar zeggen dat met het ‘blote oog’ geen leukemie meer te zien is, wat echter niet betekent dat er geen kwaadaardige cellen in het lichaam zijn achtergebleven. Als namelijk op dit moment met de behandeling gestopt zou worden, komt de leukemie altijd terug.
Daarom wordt de inductiekuur gevolgd door twee consolidatiekuren. Een consolidatiekuur ‘consolideert’, bevestigt als het ware wat met de inductiekuur is bereikt. Dankzij deze consolidatiekuren wordt de kans dat de leukemie alsnog terugkomt verder verkleind. De consolidatiekuren volgen hetzelfde principe als de inductiekuur: een aantal dagen chemotherapie gevolgd door een risicovolle wachtperiode zonder afweer.
Aan het eind van deze behandeling blijft er nog steeds een grote kans bestaan dat de leukemie niet radicaal weg is en in de komende één tot twee jaar weer terugkomt. Daarom wordt bij voorkeur de behandeling afgesloten met een behandeling bestaande uit zeer hoge dosis chemotherapie gevolgd door teruggave van stamcellen (van een donor of van de patiënt zelf), een zogenaamde stamceltransplantatie.
Hulp en ondersteuning tijdens en na therapie
Patiëntenvereniging
Veel patiënten hebben baat bij contact met de patiëntenvereniging, welke zich bevindt binnen de overkoepelende patientenvereniging HEMATON voor patiënten met bloedkanker, lymfklierkanker, multipel myeloom en voor patiënten die een stamceltransplantatie hebben ondergaan.
Stichting Hematon
Postbus 8152
3503 RD Utrecht
Tel. 030-760 34 60
E-mail: secretariaat@hematon.nl
Website: www.hematon.nl
Deze vereniging zet zich in voor alle patiënten met leukemie, dat wil zeggen acute leukemie (ALL en AML) maar ook de verschillende vormen van chronische leukemie.
Revalidatieprogramma Herstel & Balans
Daarnaast is er voor patiënten die de behandeling achter de rug hebben en moeite hebben de draad weer op te pakken, de mogelijkheid gebruik te maken van het revalidatieprogramma Herstel & Balans. Dit programma is op zestig locaties in Nederland beschikbaar, onder meer ook in het UMCG, via het Centrum voor Revalidatie, locatie Beatrixoord. Dit programma is gericht op het verminderen van klachten zoals vermoeidheid, pijn, angst en neerslachtigheid. Daardoor verbetert de kwaliteit van leven.
Een (ex-)patiënt kan aan Herstel & Balans deelnemen nadat de behandelingen tegen kanker zijn afgerond. Bij de start van de revalidatie moet de conditie zodanig zijn dat de persoon zich redelijk kan bewegen en aan het groepsprogramma kan deelnemen. De arts kan de patiënt verwijzen naar Herstel & Balans als de behandeling is afgerond en de kans op herstel aannemelijk is.
Veel zorgverzekeraars vergoeden de revalidatie via de aanvullende verzekering.
Nazorg: Het Behouden Huys
Het valt niet altijd mee om met een ziekte als kanker om te gaan. Er komt verschrikkelijk veel op je af. Eerst de klap van de diagnose, dan de vaak ingrijpende medische behandelingen. En hoe verder daarna? Hoe ga je bijvoorbeeld om met een veranderd lichaam, met vermoeidheid of een onzeker levensperspectief? Het kan daarom heel wenselijk zijn om na(ast) de medische zorg gebruik te maken van extra ondersteuning door Het Behouden Huys.
Het Behouden Huys is gelegen op het prachtige landgoed De Vijverberg te Haren. Het is een bijzondere plek waar kankerpatiënten en hun naasten onder professionele en vooral ook betrokken begeleiding stil kunnen staan bij de lichamelijke, psychische en sociale gevolgen van hun ziekte. Er is begeleiding mogelijk voor iedereen, ongeacht de leeftijd, ziektefase, prognose of het stadium van het ziekteproces.
Wilt u meer weten, zie dan: www.behoudenhuys.nl.
Acute promyelocytenleukemie (APL)
Deze vorm van acute leukemie wordt ook wel acute myeloïde leukemie met translocatie t(15;17) genoemd en wordt gerekend tot een vorm van acute leukemie met een veel betere geneeskans. In Nederland is deze vorm van acute leukemie zeldzaam, circa 5 tot 8 procent van alle acute myeloïde leukemieën. In Zuid-Europa komt deze leukemie vaker voor. Vandaar dat de behandelingsresultaten ook vooral van Spaanse en Italiaanse groepen komen. Vaak kan de diagnose snel gesteld worden, omdat de bloed- en beenmergpreparaten zeer kenmerkend zijn met een beeld van veel promyelocyten met insluitsels: auerstaven in grote aantallen, die er als ‘takkenbossen’ uitzien (zie dia 3). Er zijn afwijkende vormen van promyelocytenleukemie, maar ook die kunnen door een ervaren laboratorium goed herkend worden.

Dia 1

Dia 2
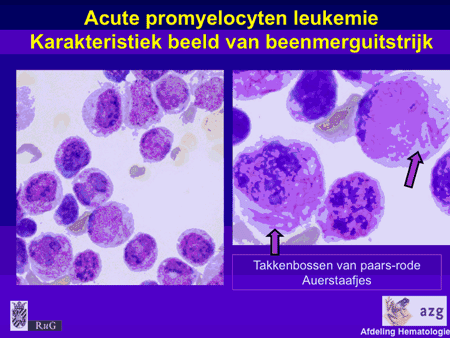
Dia 3
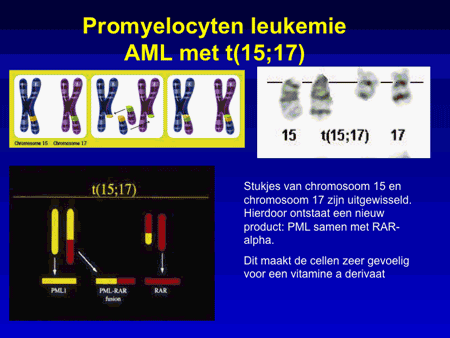
Dia 4
In acute promyelocytenleukemie is een specifieke afwijking aanwezig (een uitwisseling van twee stukjes chromosoom tussen chromosoom 15 en 17) waardoor de cellen niet verder kunnen uitrijpen (zie dia 4). Ze blijven als het ware hangen in het stadium van de promyelocyt, dat wil zeggen tussen een onrijpe cel (de myeloblast) en de rijpe granulocyt. Bij deze chromosoomtranslocatie is onder meer een receptor van vitamine A (RAR-alpha, de retinoic acid receptor alpha) betrokken. Door deze cellen te behandelen met megadoses van een afgeleide van vitamine A (ATRA, afgeleid van all-transretinoic acid), worden de cellen geforceerd uitgerijpt en gaan ze uiteindelijk dood.
Patiënten met een acute promyelocytenleukemie kunnen zich net zo presenteren als patiënten met een ‘gewone’ acute myeloïde leukemie, zoals hierboven beschreven. Een extra kenmerk is echter dat patiënten soms ernstige stollingsproblemen kunnen hebben, waardoor levensgevaarlijke bloedingen kunnen ontstaan. Deze bloedingen worden waarschijnlijk veroorzaakt door stoffen die uit de kwaardaardige promyelocyten vrijkomen. Ook in het begin van de behandeling bestaat een verhoogd risico op bloedingen wanneer de cellen doodgaan.
De behandeling van patiënten met een acute promyelocytenleukemie dient snel te beginnen, hoe eerder hoe liever. De behandeling volgt hetzelfde principe als de behandeling van patiënten met een ‘gewone’ acute myeloïde leukemie en zal bestaan uit een aantal opeenvolgende kuren. In meerdere zaken echter wijkt de behandeling af:
- De chemotherapie is bij de eerste kuren minder zwaar.
- Aan de behandeling wordt van meet af aan ATRA (Vesanoid) toegevoegd.
- Vrijwel alle patiënten zullen na afloop van enkele kuren nog een onderhoudsbehandeling krijgen van enkele jaren met een combinatie van lichte chemotherapie (mercaptopurine en methotrexaattabletten) en ATRA.
- Gezien de uitstekende prognose zal er in principe geen stamceltransplantatie nodig zijn.
De overlevingskansen van acute promyelocytenleukemie zijn uitstekend (zie dia 5). Afhankelijk van enkele risicofactoren, die voornamelijk bepaald worden door het aantal witte bloedcellen (leukocyten) en de bloedplaatjes bij de start van de ziekte, varieert de geneeskans van boven de 75 tot zelfs 100 procent. Het merendeel van de patiënten zal na afloop van de eerste kuren zijn of haar werkzaamheden kunnen hervatten, ook tijdens de onderhoudsbehandeling. Ook wanneer ondanks alles weer ziekteactiviteit ontstaat (recidief van de ziekte), is er een tweede grote kans op genezing door toevoeging van andere nieuwe medicijnen, waaronder het middel arsenicumtrioxide (afgekort als ATO), dat samen met ATRA opnieuw de ziekte onder controle zal krijgen bij 85-90% van de patiënten. Wel zal in dat geval overwogen worden of een stamceltransplantatie zinvol is om toe te voegen.
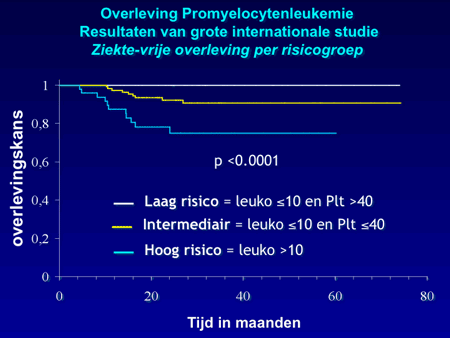
Dia 5

Dia 6
Conclusie
Promyelocytenleukemie is een zeldzame variant van acute myeloïde leukemie (AML). De kans op genezing is zeer groot. Het is van groot belang zo snel mogelijk met behandeling te starten gezien het risico op ernstige bloedingen gedurende de eerste dagen van de ziekte.
Meer weten?
Veel patiënten hebben baat bij contact met de patiëntenvereniging, welke zich bevindt binnen de overkoepelende patientenvereniging HEMATON voor patiënten met bloedkanker, lymfklierkanker, multipel myeloom en voor patiënten die een stamceltransplantatie hebben ondergaan.
Stichting Hematon
Postbus 8152
3503 RD Utrecht
Tel. 030-760 34 60
E-mail: secretariaat@hematon.nl
Website: www.hematon.nl
Deze vereniging zet zich in voor alle patiënten met leukemie, zowel acute leukemie als ook de verschillende vormen van chronische leukemie.




