Diagnose
De diagnose chronisch lymfatische leukemie (CLL) wordt vermoed op basis van lymfocytose van > 5 × 109/l, waarbij de lymfocyten een typische kernstructuur vertonen (‘grumelé-patroon’) en kapotgestreken lymfocyten (‘gumprechtse schollen’); vooral in gevorderde stadia is er ook lymfadenopathie en splenomegalie mogelijk.
De diagnose wordt bevestigd middels flowcytometrie van het bloed, waarbij > 5 × 109/l monoclonale B-cellen met specifiek fenotype worden gevonden (Matutes score, zie immuunfenotypering). Als het aantal monoclonale CD5+ B-cellen < 5 × 109/l bedraagt zonder lymfadenopathie en zonder organomegalie, is er mogelijk sprake van een monoclonale B-cellymfocytose (MBL), een mogelijke voorfase van CLL, die in ongeveer 1% per jaar evolueert naar CLL (1).
De diagnose kleincellig lymfocytair lymfoom (small lymphocytic lymphoma SLL) kan gesteld worden bij lymfadenopathie en/of splenomegalie en < 5 × 109/l monoklonale B-cellen in het perifere bloed met passende immunofenotypering.
Op basis van vnl. chromosomenonderzoek middels FISH dan wel SNP-array, mutatiestatus van de immuunglobulinegenen en ZAP70-expressie kunnen twee subgroepen onderscheiden worden, een met indolent beloop (mediane overleving > 15 jaar) en een met ongunstige prognose (mediane overleving +/- 6 jaar).
Evolutie van CLL
- Prolymfocytic transformatie (CLL/PL) (i.e. > 10% prolymfocyten in bloed); deze entiteit is anders dan de primair B-PLL (i.e. > 55% prolymfocyten in bloed);
- Transformatie naar grootcellig lymfoom (90% van de gevallen van een Richterse transformatie, RS’), suggestief van genomic instabiliteit: bloed en beenmerg blijven vaak CLL-beeld vertonen, terwijl lokaal (mediastinum/abdominaal) een grootcellig lymfoom ontstaat; in ongeveer 80% DLBCL-RS is er een klonale relatie met de oorspronkelijke CLL. Klonaal gerelateerde casussen hebben een mOS rond 12 maanden terwijl de niet-klonaal gerelateerde casussen een mOS van 65 maanden hebben. Immunofenotypisch, DLBCL-RS verliezen vaker de expressie van CD5 en CD23.
- Transformatie naar een Hodgkin-like lymfoom (10% van de gevallen van een Richterse transformatie). Ze worden behandeld als HL.
Onderzoek
Onderzoek bij diagnose:
- anamnese: WHO, B-symptomen, infecties, medicatie, cardiovasculaire voorgeschiedenis;
- lichamelijk onderzoek: aandacht voor splenomegalie, lymfadenopathie, infecties;
- bloedbeeld, handdiff (Gumprechtse Schollen c.q. smudge cells en prolymfocyten);
- lever- en nierfunctie, totaal eiwit en albumine; immuunfixatie en immuunglobulines kwantitatief;
- haptoglobine, Coombs test; reticulo’s;
- β2-microglobuline (> 2× normaal, i.e. > 4,5 mg/l, ongunstig);
- hepatitis B en C serologie;
- immuunfenotypering middels flowcytometrie (FCM) van perifeer bloed: typisch zijn B-cellen met fenotype CD19+CD5+CD23+ en zwakke expressie van CD20 en zware en lichte Ig-ketens (Matutes score); bij ‘atypische CLL’ kan het fenotype iets afwijken, bijv. sterkere expressie van Ig; CD38-positiviteit in > 20% der cellen is prognostisch ongunstig;
- niet obligaat, tenzij in studies: cristabiopsie of bij anemie en trombopenie om te differentiëren tussen beenmergverdringing of auto-immuunfenomeen; klierbiopsie alleen bij twijfel over diagnose; beeldvorming: CT-hals/thorax/abdomen alleen als lichamelijk onderzoek niet toereikend is en bijv. bij verdenking hoge ziekteload (met kans op tumorlyse);
- genetische analyse (cytogenetica, FISH, SNP-array, NGS): alleen bij behandelindicatie.
Stadiumindeling
Volgens Rai en Binet
| Stadium | Definitie |
|---|---|
| Rai | |
| Laag risico | |
| Rai 0 | Lymfocytose > 5 × 109/l |
| Intermediair risico | |
| Rai I | Lymfocytose en lymfadenopathie |
| Rai II | Lymfocytose en hepato-/splenomegalie met/zonder lymfadenopathie |
| Hoog risico | |
| Rai III | Lymfocytose en Hb < 6.9 mmol/l* met/zonder lymfadenopathie/organomegalie |
| Rai IV | Lymfocytose en trombocytopenie < 100 × 109/l* met/zonder lymfadenopathie/organomegalie |
| Binet | |
| Binet A Binet B Binet C |
Hb ≥ 6,2 mmol/l, trombocyten ≥ 100 × 109/l, < 3 lymfeklierstations Hb ≥ 6,2 mmol/l, trombocyten ≥ 100 × 109/l, ≥ 3 lymfeklierstations Hb < 6,2 mmol/l, trombocyten < 100 × 109/l* |
* indien anemie en trombocytopenie niet veroorzaakt wordt door auto-antistoffen
Prognose
Prognostische factoren zijn afhankelijk van type behandeling:
- CLL cellen met 17p deletie, TP53 mutatie of ongemuteerde IGHV status (> 2%) en/of complexe karyotype, zijn genetisch instabieler en daarmee (on)gevoelig voor chemo-immunotherapie.
CLL-IPI risicoscore (3)
| Variabele | Punten |
|---|---|
| TP53-mutatie en/of 17p deletie | 4 |
| IGHV ongemuteerde status | 2 |
| Beta2-microglobuline > 3,5 mg/l | 2 |
| Binet stadium B/C of Rai stadium I-IV | 1 |
| Leeftijd > 65 jaar | 1 |
| Prognostische score | 5-jrs OS, % |
| Laag, 0-1 | 93,2 |
| Intermediair, 2-3 | 79,4 |
| Hoog, 4-6 | 63,6 |
| Zeer hoog, 7-10 | 23,3 |
Aangezien de CLL-IPI score vooralsnog geen invloed heeft op therapiekeuze, is het niet noodzakelijk deze buiten studieverband te bepalen.
Behandeling
Filter trials en protocollen voor dit ziektebeeldCriteria voor actieve ziekte
Minstens één van de volgende criteria dient aanwezig te zijn:
| 1 | Minstens één van de volgende ziektegerelateerde symptomen: a. Gewichtsverlies ≥ 10% in voorafgaande 6 maanden b. Extreme vermoeidheid (WHO performance status ≥ 2) c. Koorts ≥ 38,6 °C gedurende ≥ 2 weken, in afwezigheid van infecties d. Nachtzweten gedurende meer dan een maand zonder aanwijzing voor infectie |
| 2 | Toenemend beenmergfalen, zich uitend in ontwikkeling van of verergering van anemie en/of trombocytopenie |
| 3 | Auto-immuun anemie en/of trombocytopenie die slecht reageert op behandeling met steroïden |
| 4 | Massale (> 6 cm onder linker ribbenboog) of progressieve splenomegalie |
| 5 | Massale klieren of pakketten (> 10 cm in grootste diameter) of progressieve lymfadenopathie |
| 6 | Progressieve lymfocytose met een stijging > 50% binnen 2 maanden, of een geanticipeerde verdubbelingstijd van minder dan 6 maanden |
Indicaties voor start behandeling
| Behandeling Rai 0 of Binet A | Nee |
| Behandeling Rai I/II of Binet B | Mogelijk (indien actieve ziekte) |
| Behandeling Rai III/IV of Binet C | Ja |
Keuze tussen behandelmodaliteiten
Aspecten om overwogen te worden:
- behandelduur: 6 maanden (chemo-immunotherapie), 24 maanden (Ven-R), tot aan progressie (ibrutinib, venetoclax monotherapie)
- comorbiditeit en bijwerkingen (bloedingsrisico, cardiovasculaire comorbiditeit bij ibrutinib vs. verminderde nierfunctie bij venetoclax)
- therapietrouw (oraal of i.v.)
- behandelzwaarte
- respons en bijwerkingen van eerdere therapie
- voorkeur van patiënt/e
Eerstelijnstherapie
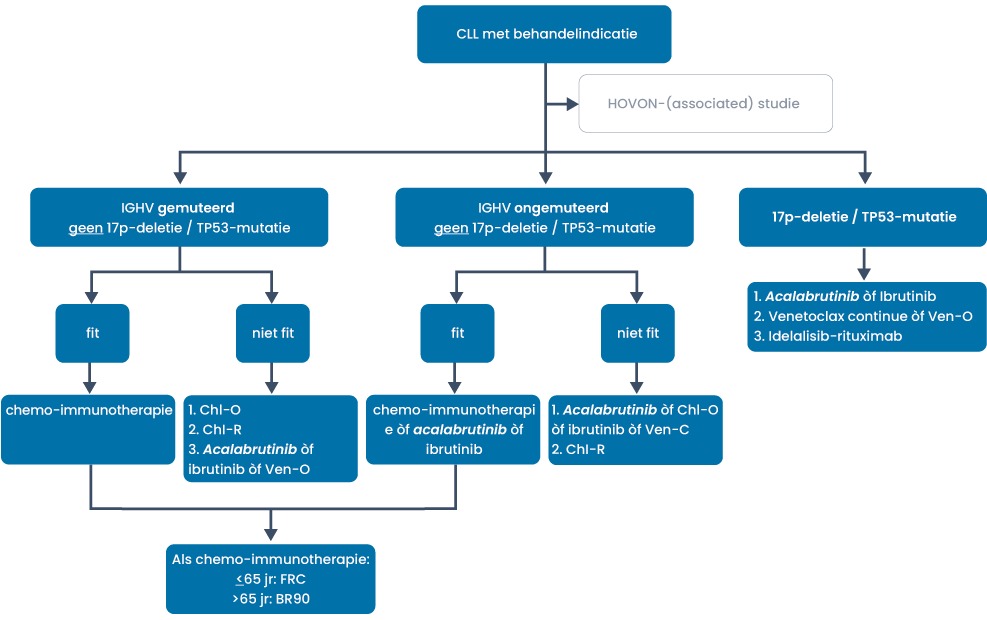
Tweedelijnstherapie in studieverband
Geopende clinical trials
GTC3013-03 (Genmab03): voor R/R CLL of Richterse syndroom
Phase 1b/2, Open-Label, Safety and Efficacy Study of Epcoritamab (GEN3013; DuoBody®-CD3 X CD20) in Relapsed/Refractory Chronic Lymphocytic Leukemia and Richter’s Syndrome
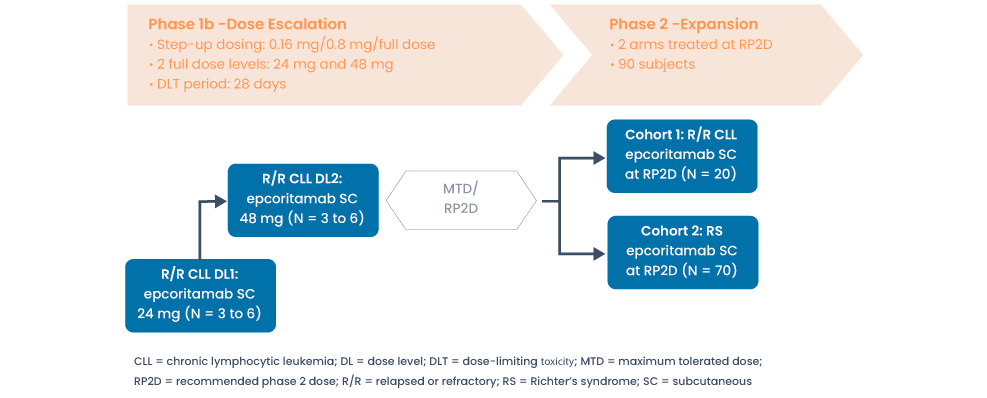
HOVON 159 (REVEAL)
REtreatment with VEnetoclax and Acalabrutinib after venetoclax Limited duration (REVEAL.)
A prospective, multicenter, phase-II trial of venetoclax plus acalabrutinib in patients who have relapsed after first line venetoclax + anti-CD20 mAb treatment for chronic lymphocytic leukemia (CLL or SLL)
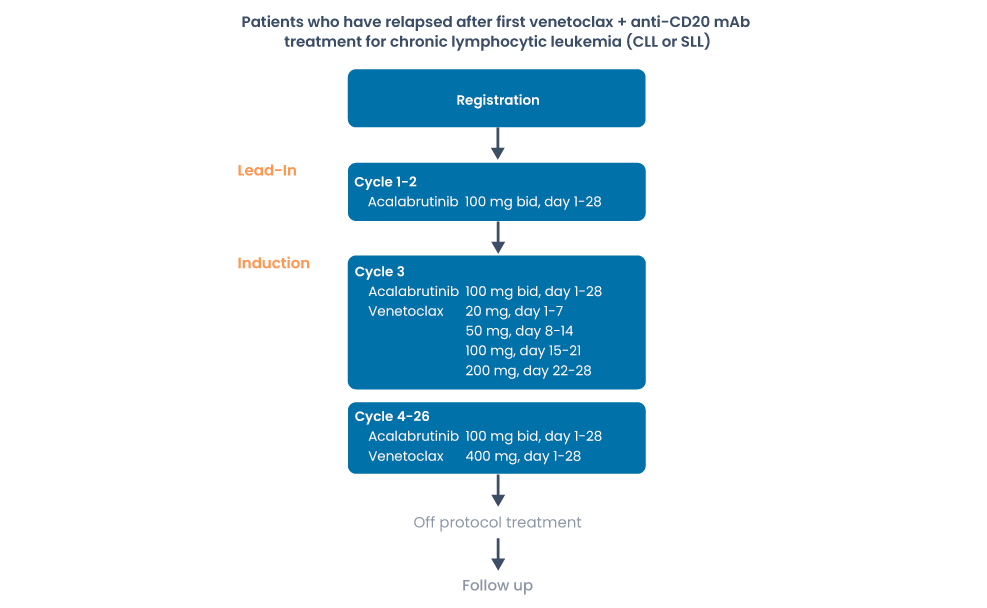
Tweedelijnstherapie buiten studieverband
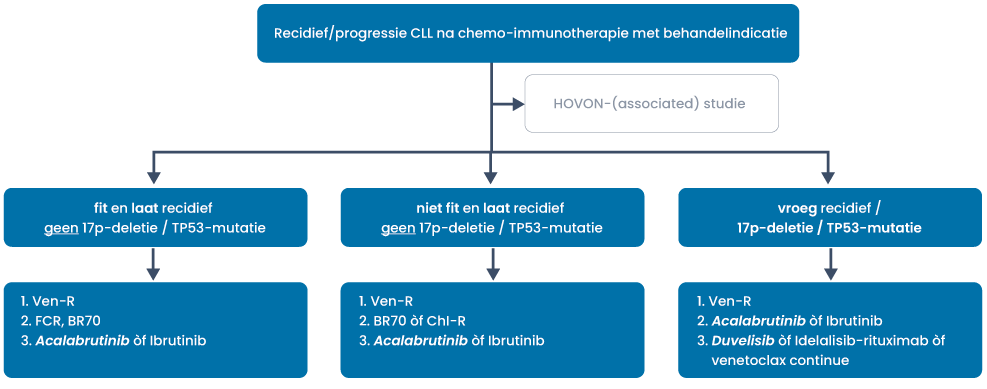
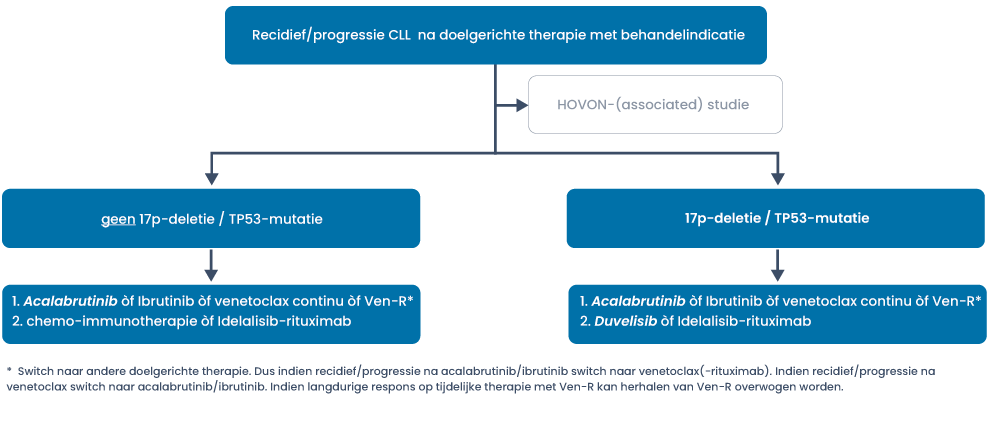
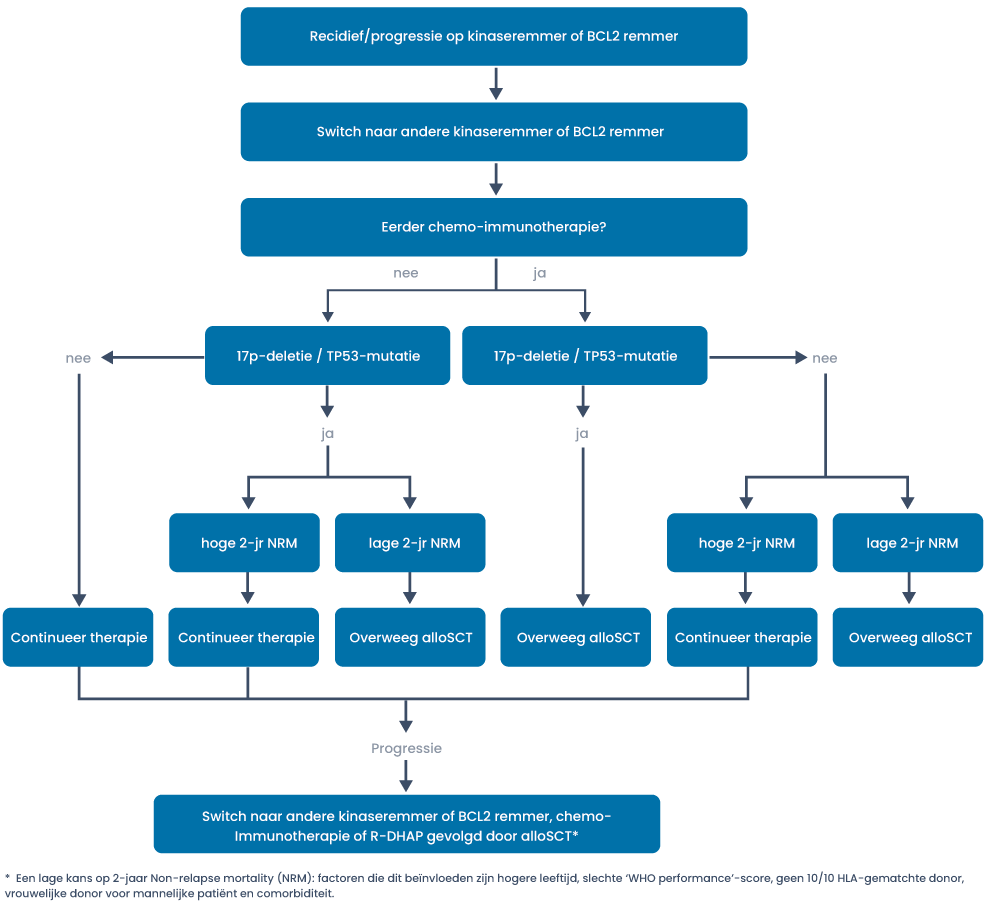
Indicaties voor allogene stamceltransplantatie
Kuurschema’s
| FCR, streef 6 cycli | Fludarabine 40 mg/m2 per os dag 1-3, à 4 weken óf Fludarabine 25 mg/m2 i.v. dag 1-3, à 4 weken |
| Cyclofosfamide 250 mg/m2 per os dag 1-3, à 4 weken | |
| Rituximab: eerste infusie 375 mg/m2 dag 1, daarna 500 mg/m2 dag 1, à 4 weken | |
| Bendamustine-Rituximab (BR90), streef 6 cycli, 1e lijn | Bendamustine 90 mg/m2 i.v. dag 1-2, à 4 weken |
| Rituximab: eerste infusie 375 mg/m2 dag 1, daarna 500 mg/m2 dag 1, à 4 weken | |
| Bendamustine-Rituximab (BR70), streef 4-6 cycli, 2e lijn | Bendamustin 70 mg/m2 i.v. dag 1-2, à 4 weken |
| Rituximab: eerste infusie 375 mg/m2 dag 1, daarna 500 mg/m2 dag 1, à 4 weken | |
| Chloorambucil voorkeursschema, streef 6 cycli | Chloorambucil 10 mg/m2 per os dag 1-7, à 4 weken |
| Chloorambucil alternatieve schema’s | Chloorambucil 0,1-0,15 mg/kg/d per os continu, tot maximale respons, maximaal 1 jaar Chloorambucil 10 mg per os dag 1-14, à 4 weken Chloorambucil 0,4 mg/kg per os dag 1-14, à 4 weken Chloorambucil 20 mg dag per os, dag 1-5, à 4 weken Chloorambucil 0,5 mg/kg per os, dag 1 en 15, à 4 weken |
| Anti-CD20 (in combinatie met chloorambucil), streef 6 cycli | Obinutuzumab, cyclus 1 eerste infusie 100 mg + 900 mg dag 1, 2, daarna 1000 mg dag 8 en 15, cyclus 2-6 1000 mg à 4 weken |
| Rituximab: eerste infusie 375 mg/m2 dag 1, daarna 500 mg/m2 dag 1, à 4 weken | |
| Ibrutinib | 1 × daags 420 mg per os, continu tot aan progressie (advies: 1e 6 maanden 3 × 140 mg, bij stabiel ingesteld 1 × 420 mg) |
| Acalabrutinib | 2 × daags 100 mg per os, continu tot aan progressie |
| Venetoclax – Obinutuzumab (12 cycli) | Obinutuzumab, cyclus 1 eerste infusie 100 mg + 900 mg dag 1, 2, daarna 1000 mg dag 8 en 15, cyclus 2-6 1000 mg à 4 weken |
| Venetoclax 20 mg 1 × daags (cyclus 1, dag 22-28) Venetoclax 50 mg 1 × daags (cyclus 2, dag 1-7) Venetoclax 100 mg 1 × daags (cyclus 2, dag 8-14) Venetoclax 200 mg 1 × daags (cyclus 2, dag 15-21) Venetoclax 400 mg 1 × daags (cyclus 2, dag 22-28) Venetoclax 400 mg 1 × daags (cyclus 3-12, dag 1-28) |
|
| Venetoclax – Rituximab (24 cycli) | Rituximab (dus pas starten na 5 weken dosis opbouw van venetoclax): eerste infusie 375 mg/m2 (cyclus 1), daarna 500 mg/m2 (in cyclus 2-6) dag 1, à 4 weken |
| Venetoclax 20 mg 1 × daags (dosis opbouw, dag 1-7) Venetoclax 50 mg 1 × daags (dosis opbouw, dag 8-14) Venetoclax 100 mg 1 × daags (dosis opbouw, dag 15-21) Venetoclax 200 mg 1 × daags (dosis opbouw, dag 22-28) Venetoclax 400 mg 1 × daags (dosis opbouw, dag 28-35) Venetoclax 400 mg 1 × daags (cyclus 1-24, dag 1-28) |
|
| Venetoclax monotherapie (tot aan progressie) | Venetoclax 20 mg 1 × daags (dag 1-7) Venetoclax 50 mg 1 × daags (dag 8-14) Venetoclax 100 mg 1 × daags (dag 15-21) Venetoclax 200 mg 1 × daags (dag 22-28) Venetoclax 400 mg 1 × daags (vanaf dag 29 tot aan progressie) |
| Idelalisib continu, Rituximab (max. 8 keer) | 2 × daags 150 mg per os, continu tot aan progressie |
| Rituximab week 1: 375 mg/m2 dag 1, week 3, 5, 7, 9, 13, 17, 21: 500 mg/m2 dag 1 | |
| R-DHAP, 1-3 kuren, streef ten minste PR | Dexamethason 40 mg per os of i.v. dag 1-4, à 4 weken Cisplastin 100 mg/m2 i.v. dag 1 Cytarabine 2000 mg/m2 i.v. à 12 uur dag 2 |
| Rituximab: eerste infusie 375 mg/m2, daarna 500 mg/m2 | |
| HD-methylprednisolon-rituximab (max. 3 keer) | HD-methylprednisolon 1 g/m2 i.v. dag 1-5, à 4 weken |
| Rituximab: 375 mg/m2, dag 1, 3, 5, 8, 17 en 22 (cyclus 1), dag 1, 7, 14, 21 (cyclus 2-3) |
Aanbevelingen bij complicaties
Venetoclax
Tumorlyse-preventie bij venetoclax
| TLS risicocategorie | grootste diameter van alle meetbare lymfeklieren | absolute lymphocyte count (ALC) | GFR | ||
|---|---|---|---|---|---|
| laag | < 5 cm | EN | < 25 × 109/l | EN | > 50 ml/min |
| intermediair | > 5 cm en < 10 cm | OF | ≥ 25 × 109/l | EN | > 50 ml/min |
| hoog | > 5 cm en < 10 cm | EN | ≥ 25 × 109/l | OF | 30-50 ml/min |
| > 10 cm | Irrelevant |
| TLS risicocategorie | Voorzorgsmaatregelen | Laboratoriumbepaling*** | |
| Hydratie | Anti-hyperuricemics | Setting en frequentie van laboratoriumbepalingen | |
| Laag | Oraal (1,5-2 l)* | Allopurinol** | Poliklinisch:
|
| Intermediair | Oraal (1,5-2 l)* en overweeg intraveneus op dagen van start venetoclax en bij 1e ophoging naar 50 mg venetoclax |
Allopurinol** | Poliklinisch:
|
| Hoog | Oraal (1,5-2 l)* en intraveneus (100-200 ml/hr) tot in ieder geval 24 uur na 1e gift van 20 mg en 50 mg |
Allopurinol** Rasburicase wordt aanbevolen indien urinezuur is verhoogd** |
Klinische opname bij start van 1e gift van 20 mg en 50 mg
|
* Gedurende de gehele ramp-up periode.
** Allopurinol moet niet worden gegeven op dagen van rasburicase.
*** De volgende laboratoriumbepalingen dienen bepaald te worden:
Vóór start van elke ophoging in dosering: hemoglobine, leukocyten, trombocyten, natrium, kalium, calcium, albumine, fosfaat, urinezuur, kreatinine en LDH.
6 tot 8 uur (én 24 uur) na elke 1e gift van opgehoogde dosering: kalium, calcium, fosfaat, urinezuur en creatinine.
Ibrutinib
Verhoogd bloedingsrisico bij ibrutinib:
- Absolute contra-indicatie voor ibrutinib indien gebruik van vitamine-K-antagonist of DOAC in combinatie met een trombocytenaggregatieremmer of indien dubbele trombocytenaggregatieremmers
- Switch bij voorkeur vitamine-K-antagonisten naar een DOAC
- Staak ibrutinib, 3-7 dagen, rondom invasieve ingrepen
- Staak ibrutinib bij een ernstige bloeding en dien trombocytentransfusie toe, ibrutinib dient afgebouwd te worden bij patiënten die recent gestart zijn (< 6 maanden na start), om flare-up van CLL te voorkomen
Atriumfibrilleren bij ibrutinib:
- Ibrutinib kan gecontinueerd worden bij atriumfibrilleren (gebruik bij voorkeur een bètablokker als anti-aritmica (gezien interactie van andere aritmica en ibrutinib))
- Start bij voorkeur een DOAC als antistolling noodzakelijk is
Hypertensie bij ibrutinib:
- Controleer bij elk polibezoek de bloeddruk en behandel zo nodig met een anti-hypertensivum
Omgaan ten aanzien van CYP3A4-remmers en inductoren bij ibrutinib
- Absolute contra-indicatie voor sterke CYP3A4-remmers, zoals ketaconazol
- Relatieve contra-indicatie voor CYP3A4-remmers, zoals verapamil, diltiazem, amiodarone, voriconazol, itraconazol en P-glycoproteïne-substraten zoals digoxine. Overweeg dosisreductie van ibrutinib
Infecties bij ibrutinib:
- Overweeg tijdens een ernstige infectie ibrutinib tijdelijk te staken (pas op voor flare-up bij recent starten van ibrutinib, zie hierboven)
Idelalisib
Diarree en pneumonitis bij idelalisib:
- Staak idelalisib bij gr 1-2 diarree, die langer dan 3 dagen aanhoudt en bij gr 3-4 diarree.
- Staak idelalisib zo nodig bij longklachten en hoge resolutie CT-afwijkingen niet passend bij lobaire pneumonie.
- Dien zo nodig corticosteroïden toe.
Transaminitis bij idelalisib:
- Monitor frequent ASAT en ALAT, met name in de 1e 3 maanden.
- Staak zo nodig idelalisib of dien corticosteroïden toe.
Algemeen
Infectiepreventie:
- PJP profylaxe met cotrimoxazol 1 dd 480 mg, tot 6 maanden na FCR, bendamustine-rituximab en idelalisib-rituximab
- Herpesprofylaxe op indicatie volgens lokale protocol
- Geen standaard PJP, herpes en anti-schimmel profylaxe bij ibrutinib en venetoclax
- Monitoring CMV-infectie bij idelalisib, bijvoorbeeld 1× per maand
Bestraalde bloedproducten tot 1 jaar na FCR
Warmte auto-immuun anemie of trombocytopenie:
- Prednison 1 mg/kg: 1 mg/kg/dag p.o. gedurende tenminste 3 weken. Bij het bereiken van een (sub)normaal Hb wordt de prednison met 10-15 mg/week uitgeslopen naar 30 mg/dag.
Daarna reductie tot 15 mg met 5 mg/week en verder uitsluipen door met 2,5 mg/week te verlagen, regelmatig controleren of hemolyse ontstaat/verergert en uitsluipen vertragen (of CLL-therapie starten). - Indien geen respons op prednison: Rituximab 4 × 375 mg/m2 à 1 week (alternatief splenectomie) (SORT C)
- Indien geen respons op rituximab: CLL-behandeling (alternatief splenectomie)
Koude antistoffen hemolytische anemie:
- Rituximab 4 × 375 mg/m2 à 1 week
- Indien geen respons op rituximab: CLL-behandeling
Immuun cytopenie na purine-analogen:
- Staken purine-analogen, start prednison 1 mg/kg
- Indien geen verbetering: overweeg ciclosporine toevoegen
Recidiverende luchtweginfecties
Bij recidiverende infecties wordt naast diagnostiek antibiotica on demand aanbevolen. In het geval van ≥ 3 infecties per jaar is profylactisch antibiotica aangewezen: cotrimoxazol 1 dd 960 mg, azitromycine 3 keer per week 250 mg of doxycycline 1 dd 100 mg
Hypogammaglobulinemie:
Overweeg immunoglobuline suppletie bij:
- hypogammaglobulinemie en recidiverende infecties ≥ 3 × per jaar ondanks profylactische antibiotica
- hypogammaglobulinemie en complicaties van recidiverende infecties zoals longschade (bronchiëctasieën)
| Gewicht | Dosering IVIG | Interval |
|---|---|---|
| 50 kg | 10 g | 4 weken |
| 55 kg | 10 g | 3 weken |
| 60 kg | 10 g | 3 weken |
| 65 kg | 15 g | 4 weken |
| 70 kg | 15 g | 4 weken |
| 75 kg | 15 g | 4 weken |
| 80 kg | 15 g | 3 weken |
| 85 kg | 15 g | 3 weken |
| 90 kg | 20 g | 4 weken |
| 95 kg | 20 g | 4 weken |
| 100 kg | 20 g | 4 weken |
Dosering immuunglobulines: 100 mg/kg/week of 200-400 mg/kg per 3-4 weken. i.v. toediening of subcutane toediening is mogelijk. Streef een dalspiegel in geval van recidiverende infecties > 6 g/l of bij aanhoudende infecties en/of bij structurele schade (bronchiëctasieën) > 8 g/l.
Therapie-evaluatie: het effect van immuunglobulinesuppletie na 6 maanden tot 1 jaar evalueren. Indien de infecties onder controle zijn kan een dosisverlaging of op proef staken overwogen worden. Bij patiënten met complicaties is levenslange immuunglobulinesuppletie geïndiceerd.
Vaccinaties
Zie voor aanbevolen vaccinaties, richtlijn RIVM24.
Symptomatische lymfadenopathie bij patiënt met contra-indicatie voor systemische therapie: Radiotherapie 2×2 Gy
Literatuurlijst
- Rawston, A.C., Bennett, F.L., OÇonnor, S.J., et al. Monoclonal B-cell lymphocytosis and chronic lymphocytic leukaemia. NEJM 2008, 359, 638-40.




